Dodanie nukleofili węglowych
Szeroka gama nukleofili węglowych dodaje się do aldehydów i takie reakcje mają pierwszorzędne znaczenie w syntetycznej chemii organicznej, ponieważ produkt stanowi połączenie dwóch szkieletów węglowych. Chemicy organiczni byli w stanie zmontować prawie każdy szkielet węglowy, bez względu na to, jak skomplikowany, dzięki pomysłowemu wykorzystaniu tych reakcji. Jednym z najstarszych i najważniejszych jest dodanie odczynników Grignarda (RMgX, gdzie X oznacza atom halogenu). Francuski chemik Victor Grignard zdobył Nagrodę Nobla z 1912 roku w dziedzinie chemii za odkrycie tych odczynników i ich reakcji.
Dodanie odczynnika Grignarda do aldehydu, a następnie zakwaszenie w wodnym kwasie daje alkohol. Dodatek do formaldehydu daje pierwszorzędowy alkohol. Dodatek do aldehydu innego niż formaldehyd daje alkohol drugorzędowy.
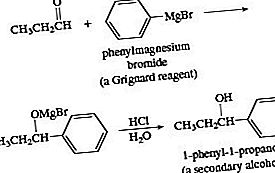
Innym nukleofilem węglowym jest jon cyjankowy, CN -, który reaguje z aldehydami, po zakwaszeniu dając cyjanohydryny związki zawierające grupę OH i CN na tym samym atomie węgla.
Cyjanohydryna benzaldehydowa (mandelonitryl) stanowi interesujący przykład mechanizmu obrony chemicznej w świecie biologicznym. Substancja ta jest syntetyzowana przez krocionogi (Apheloria corrugata) i przechowywana w specjalnych gruczołach. Gdy krocionóg jest zagrożony, cyjanohydryna jest wydzielana z gruczołu magazynowego i ulega katalizowanej enzymatycznie dysocjacji z wytworzeniem cyjanowodoru (HCN). Krocionóg uwalnia następnie gaz HCN do otaczającego środowiska, aby odeprzeć drapieżniki. Ilość HCN emitowana przez pojedynczy krocionóg jest wystarczająca do zabicia małej myszy. Mandelonitryl znajduje się również w gorzkich migdałach i pestkach brzoskwini. Jego funkcja nie jest znana.
Inne ważne reakcje w tej kategorii obejmują reakcję Knoevenagela, w której nukleofilem węgla jest ester z co najmniej jednym α-wodorem. W obecności silnej zasady ester traci α-wodór z wytworzeniem ujemnie naładowanego węgla, który następnie dodaje się do węgla karbonylowego aldehydu. Zakwaszenie, po którym następuje utrata cząsteczki wody, daje ester α, β-nienasycony.
Inną reakcją addycji z udziałem nukleofilu węgla jest reakcja Wittiga, w której aldehyd reaguje z fosforanem (zwanym także ylidem fosforu), z wytworzeniem związku zawierającego podwójne wiązanie węgiel-węgiel. Wynikiem reakcji Wittiga jest zastąpienie tlenu karbonylowego aldehydu przez grupę węglową związaną z fosforem. Niemiecki chemik Georg Wittig podzielił Nagrodę Nobla w dziedzinie chemii z 1979 r. Za odkrycie tej reakcji i rozwój jej zastosowania w syntetycznej chemii organicznej.
Związki zawierające grupę trimetylosililową (-SiMe 3, w którym Me oznacza grupę metylową, -CH 3) i litu (Li) wodoru na tym samym atomie węgla, reaguje z aldehydami w tak zwanej reakcji Peterson, uzyskując te same produkty, które być otrzymane przez odpowiednią reakcję Wittiga.
Przemieszczenie na węglu α
Halogenowanie α
Α wodoru aldehydu mogą być zastąpione przez atom chloru (Cl), bromu (Br) lub jodu (I), atom jeśli związek poddaje się działaniu Cl 2, Br 2 lub I 2, odpowiednio, albo bez katalizatora lub w obecności kwasowego katalizatora.
Reakcję można łatwo zatrzymać po dodaniu tylko jednego atomu fluorowca. Fluorowcowanie α faktycznie zachodzi w postaci enolu (patrz wyżej Właściwości aldehydów: tautomeria) aldehydu, a nie w samym aldehydzie. Ta sama reakcja zachodzi, jeśli dodaje się zasadę, ale wtedy nie można jej zatrzymać, dopóki wszystkie α-halogeny przyłączone do tego samego węgla nie zostaną zastąpione atomami halogenu. Jeżeli istnieją trzy a-atomy wodoru na tym samym atomie węgla, reakcja idzie o krok dalej, w wyniku rozszczepiania X 3 C - jonowy (gdzie X jest halogenem) i tworzenia soli kwasu karboksylowego.

Reakcja ta jest zwana reakcja haloform, ponieważ X 3 C - jonów reaguje z wodą lub innym kwasem obecnym w układzie do wytwarzają związki postaci X 3 CH, zwane haloforms (np CHCI 3 nazywa chloroform).