Konformacja, dowolna z nieskończonej liczby możliwych układów przestrzennych atomów w cząsteczce, które wynikają z rotacji jej grup atomów wokół pojedynczych wiązań.
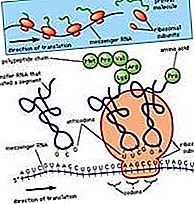
białko: Konformacja białek w interfejsach
Podobnie jak wiele innych substancji z grupami hydrofilowymi i hydrofobowymi, rozpuszczalne białka mają tendencję do migracji do granicy między powietrzem
Możliwe są różne konformacje dla dowolnej cząsteczki, w której pojedyncze wiązanie kowalencyjne łączy dwie grupy poliatomowe, w których co najmniej jeden atom nie leży wzdłuż osi danego pojedynczego wiązania. Najprostszą taką cząsteczką jest nadtlenek wodoru, w którym dwie grupy hydroksylowe mogą obracać się względem siebie wokół osi wiązania tlen-tlen. Obecność więcej niż jednej takiej pojedynczego wiązania w cząsteczce, w tym propanu (CH 3 -CH 2 -CH 3), na przykład, tylko przyczynia się do skomplikowania sytuacji bez zmiany jego naturę. W cząsteczkach, takich jak cząsteczki cyjanogenu (N≡C ― C≡N) lub butadynu (H ― C≡C ― C≡C ― H), wszystkie atomy leżą wzdłuż osi centralnego pojedynczego wiązania, dzięki czemu nie można odróżnić konformacji istnieć.
Zasadniczo każda rozpoznawalna konformacja cząsteczki reprezentuje stan o różnej energii potencjalnej z powodu działania sił przyciągających lub odpychających, które różnią się w zależności od odległości między różnymi częściami struktury. Gdyby te siły były nieobecne, wszystkie konformacje miałyby tę samą energię, a obrót wokół pojedynczego wiązania byłby całkowicie swobodny lub nieograniczony. Jeśli siły są silne, różne konformacje różnią się znacznie pod względem energii lub stabilności: cząsteczka zwykle zajmie stan stabilny (o niskiej energii) i przejdzie do innego stanu stabilnego dopiero po absorpcji wystarczającej ilości energii, aby osiągnąć i przejść przez niestabilną interweniującą struktura.
Na przykład siły wewnątrzcząsteczkowe w etanie są tak słabe, że ich istnienie można wywnioskować jedynie z subtelnego wpływu na właściwości termodynamiczne, takie jak entalpia i entropia. (Nawet jeśli rotacja wewnętrzna w etanie była poważnie ograniczona, jej trzy najbardziej stabilne konformacje są nierozróżnialne.) Struktury molekularne niektórych bardziej złożonych związków narzucają jednak tak silne bariery dla rotacji, że formy stereoizomeryczne - różniące się jedynie konformacją - są wystarczająco stabilne, aby być izolowanym.







![Oblężenie wojny osmańsko-weneckiej na Korfu [1716] Oblężenie wojny osmańsko-weneckiej na Korfu [1716]](https://images.thetopknowledge.com/img/world-history/0/siege-corfu-ottoman-venetian-war-1716.jpg)