Kwas tlenowy, dowolny kwas zawierający tlen. Większość kowalencyjnych niemetalicznych tlenków reaguje z wodą, tworząc tlenki kwasowe; to znaczy, reagują z wodą, tworząc tlenokwasy, które dają jony hydroniowe (H 3 O +) w roztworze. Istnieją pewne wyjątki, takie jak tlenek węgla, tlenek azotu, CO, N 2 O i tlenku azotu, NO.
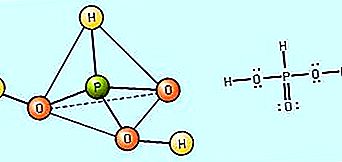
Siła kwasu tlenowego jest określona przez stopień, w jakim dysocjuje on w wodzie (tj. Jego zdolność do tworzenia jonów H +). Zasadniczo względną siłę tlenowych kwasów można przewidzieć na podstawie elektroujemności i liczby utlenienia centralnego atomu niemetalicznego. Siła kwasu wzrasta wraz ze wzrostem elektroujemności atomu centralnego. Na przykład, ponieważ elektroujemność chloru (Cl) jest większa niż siarki (S), która z kolei jest większa niż fosforu (P), można przewidzieć, że kwas nadchlorowy, HClO 4, jest silniejszym kwasem niż kwas siarkowy, H 2 SO 4, który powinien być mocniejszym kwasem niż kwas fosforowy, H 3 PO 4. Dla danego niemetalicznego atomu centralnego siła kwasu wzrasta wraz ze wzrostem liczby utlenienia atomu centralnego. Na przykład kwas azotowy, HNO 3, w którym atom azotu (N) ma liczbę utlenienia +5, jest mocniejszym kwasem niż kwas azotawy, HNO 2, gdzie stan utlenienia azotu wynosi +3. W ten sam sposób, kwas siarkowy, H 2 SO 4, z siarką w stanie utlenienia +6 jest mocniejszym kwasem niż kwas siarkawy, H 2 SO 3, w których liczba +4 utlenianie siarki istnieje.
Sól kwasu tlenowego jest związkiem powstającym, gdy kwas reaguje z zasadą: kwas + zasada → sól + woda. Ten rodzaj reakcji nazywa się neutralizacją, ponieważ roztwór jest neutralny.










![Traktat rzymski w Europie [1957] Traktat rzymski w Europie [1957]](https://images.thetopknowledge.com/img/politics-law-government/1/treaty-rome-europe-1957.jpg)
