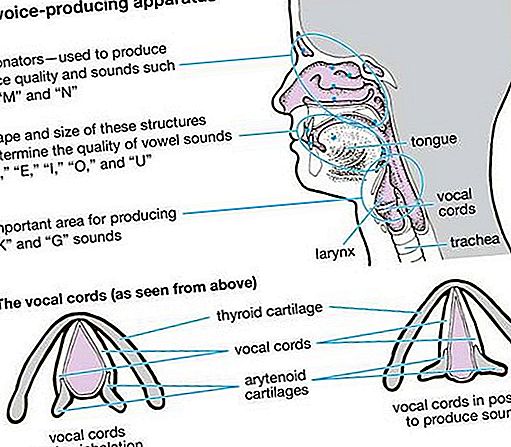
Magnez (Mg), pierwiastek chemiczny, jeden z metali ziem alkalicznych z grupy 2 (IIa) układu okresowego pierwiastków i najlżejszy metal konstrukcyjny. Jego związki są szeroko stosowane w budownictwie i medycynie, a magnez jest jednym z pierwiastków niezbędnych w całym życiu komórkowym.

metali ziem alkalicznych
oznaczają beryl (Be), magnez (Mg), wapń (Ca), stront (Sr), bar (Ba) i rad (Ra).
Właściwości elementu
| Liczba atomowa | 12 |
|---|---|
| masa atomowa | 24,305 |
| temperatura topnienia | 650 ° C (1,202 ° F) |
| temperatura wrzenia | 1 090 ° C (1 994 ° F) |
| środek ciężkości | 1,74 w 20 ° C (68 ° F) |
| stan utlenienia | +2 |
| konfiguracja elektronów | 1s 2 2s 2 2p 6 3s 2 |
Występowanie, właściwości i zastosowania
Znany pierwotnie ze związków takich jak sole Epsom (siarczan), magnezja lub magnezja alba (tlenek) i magnezyt (węglan), sam srebrzysty biały pierwiastek nie występuje w naturze jako wolny. Po raz pierwszy został wyizolowany w 1808 roku przez Sir Humphry'ego Davy'ego, który odparował rtęć z amalgamatu magnezowego wytworzonego przez elektrolizę mieszaniny wilgotnej magnezji i tlenku rtęci. Nazwa magnez pochodzi od Magnezji, dzielnicy Tesalii (Grecja), w której po raz pierwszy znaleziono mineralną magnezję alba.
Magnez jest ósmym najliczniejszym pierwiastkiem w skorupie ziemskiej (około 2,5 procent) i jest, po aluminium i żelazie, trzecim pod względem obfitości metalem konstrukcyjnym. Jego obfitość kosmiczna jest szacowana na 9,1 × 10 5 atomów (w skali, gdzie obfitość krzemu = 10 6 atomów). Występuje on w postaci węglanów-magnezytu MgCO 3 i dolomitu, CaMg (CO 3) 2 -i w wielu krzemianów wspólnych oraz talk, oliwin oraz większości rodzajów azbestu. To jest również zawarty w ługu (brucytu), chlorek (karnalit, KMgCl 3 ∙ 6H 2 O) i siarczan (kizerytu). Jest dystrybuowany w minerałach, takich jak serpentyna, chryzolit i pianka morska. Woda morska zawiera około 0,13 procent magnezu, głównie w postaci rozpuszczonego chlorku, co nadaje mu charakterystyczny gorzki smak.
Magnez jest produkowany przez elektrolizę stopionego chlorku magnezu (MgCl 2), przetworzeniu głównie z wody morskiej i do bezpośredniej redukcji jego związków z odpowiednimi środkami, przykładowo: redukujących w wyniku reakcji z tlenkiem magnezu lub kalcynowanego dolomitu z żelazokrzemu (proces Pidgeon). (Zobacz przetwarzanie magnezu.)
Pewnego razu magnezu użyto do fotograficznej wstęgi błyskowej i proszku, ponieważ w drobno rozdrobnionej postaci pali się w powietrzu intensywnym białym światłem; wciąż znajduje zastosowanie w urządzeniach wybuchowych i pirotechnicznych. Ze względu na małą gęstość (tylko dwie trzecie gęstości aluminium) znalazła szerokie zastosowanie w przemyśle lotniczym. Ponieważ jednak czysty metal ma niską wytrzymałość strukturalną, magnez stosuje się głównie w postaci stopów - głównie z 10% lub mniej aluminium, cynku i manganu - w celu poprawy jego twardości, wytrzymałości na rozciąganie i zdolności do odlewania, spawania i obrabiane maszynowo. Techniki odlewania, walcowania, wytłaczania i kucia są stosowane ze stopami, a dalsze wytwarzanie uzyskanego arkusza, płyty lub wytłaczania odbywa się poprzez normalne operacje formowania, łączenia i obróbki. Magnez jest najłatwiejszym metalem konstrukcyjnym do obróbki i był często stosowany, gdy wymagana jest duża liczba operacji obróbki. Stopy magnezu mają wiele zastosowań: są stosowane w częściach samolotów, statków kosmicznych, maszyn, samochodów, przenośnych narzędzi i urządzeń gospodarstwa domowego.
Przewodność cieplna i elektryczna magnezu oraz jego temperatura topnienia są bardzo podobne do aluminium. Podczas gdy aluminium jest atakowane przez zasady, ale jest odporne na większość kwasów, magnez jest odporny na większość zasad, ale jest łatwo atakowany przez większość kwasów w celu uwolnienia wodoru (ważne są wyjątkowe kwasy chromowy i fluorowodorowy). W normalnych temperaturach jest stabilny w powietrzu i wodzie z powodu tworzenia cienkiej ochronnej warstwy tlenku, ale jest atakowany przez parę. Magnez jest silnym środkiem redukującym i służy do produkcji innych metali z ich związków (np. Tytanu, cyrkonu i hafnu). Reaguje bezpośrednio z wieloma elementami.
Magnez występuje w naturze jako mieszanina trzech izotopów: magnezu-24 (79,0 procent), magnezu-26 (11,0 procent) i magnezu-25 (10,0 procent). Przygotowano dziewiętnaście izotopów promieniotwórczych; magnez-28 ma najdłuższy okres półtrwania, wynoszący 20,9 godziny, i jest emiterem beta. Chociaż magnez-26 nie jest radioaktywny jest nuklid aluminium-26, która ma okres półtrwania 7,2 x 10 5 lat. Podwyższone poziomy magnezu-26 stwierdzono w niektórych meteorytach, a stosunek magnezu-26 do magnezu-24 został wykorzystany do określenia ich wieku.
Najlepsi producenci magnezu w drugiej dekadzie XXI wieku to Chiny, Rosja, Turcja i Austria.