Teoria stanu przejściowego, zwana także teorią kompleksów aktywowanych lub teorią bezwzględnych szybkości reakcji, obróbka reakcji chemicznych i innych procesów, które uważają je za przebiegające przez ciągłą zmianę względnych pozycji i potencjalnych energii składowych atomów i cząsteczek. Na ścieżce reakcji między początkowym i końcowym układem atomów lub cząsteczek istnieje konfiguracja pośrednia, w której energia potencjalna ma maksymalną wartość. Konfiguracja odpowiadająca temu maksimum jest znana jako aktywowany kompleks, a jego stan nazywany jest stanem przejściowym. Różnica między energiami przejścia i stanami początkowymi jest ściśle związana z eksperymentalną energią aktywacji dla reakcji; reprezentuje minimalną energię, którą system reagujący lub przepływający musi uzyskać, aby nastąpiła transformacja. W teorii stanu przejściowego uważa się, że aktywowany kompleks został utworzony w stanie równowagi z atomami lub cząsteczkami w stanie początkowym, a zatem można określić jego właściwości statystyczne i termodynamiczne. Szybkość osiągania stanu końcowego zależy od liczby utworzonych kompleksów aktywowanych i częstotliwości, z jaką przechodzą do stanu końcowego. Ilości te można obliczyć dla prostych układów, stosując zasady statystyczno-mechaniczne. W ten sposób stała szybkości procesu chemicznego lub fizycznego może być wyrażona w kategoriach wymiarów atomowych i molekularnych, mas atomowych oraz sił międzyatomowych lub międzycząsteczkowych. Teorię stanu przejściowego można również sformułować termicznie. (Patrz kinetyka chemiczna.)
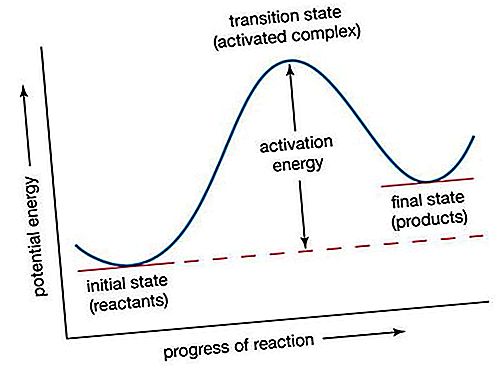

kinetyka chemiczna: teoria stanu przejściowego
Idea powierzchni energii potencjalnej wywodzi się z pomysłów holenderskiego chemika fizycznego Jacobusa Henricusa van 't Hoffa i szwedzkiego fizyka













