Krioprezerwacja, ochrona komórek i tkanek poprzez zamrażanie.

Sir Ian Wilmut: Badania edukacyjne i krioprezerwacyjne
Wilmut wychował się w Coventry, mieście w historycznym angielskim hrabstwie Warwickshire, i uczęszczał do Akademii Rolniczej na Uniwersytecie
Krioprezerwacja opiera się na zdolności niektórych małych cząsteczek do wchodzenia do komórek i zapobiegania odwodnieniu i tworzeniu się wewnątrzkomórkowych kryształków lodu, które mogą powodować śmierć komórki i zniszczenie organelli komórkowych podczas procesu zamrażania. Dwoma powszechnymi środkami krioprotekcyjnymi są dimetylosulfotlenek (DMSO) i glicerol. Glicerol jest stosowany głównie do krioprotekcji czerwonych krwinek, a DMSO służy do ochrony większości innych komórek i tkanek. Cukier zwany trehalozą, który występuje w organizmach zdolnych przetrwać ekstremalne odwodnienie, jest stosowany do liofilizacji metod kriokonserwacji. Trehaloza stabilizuje błony komórkowe i jest szczególnie przydatna do ochrony plemników, komórek macierzystych i komórek krwi.
Większość systemów kriokonserwacji komórkowej używa zamrażarki o kontrolowanej szybkości. Ten system zamrażania dostarcza ciekły azot do zamkniętej komory, w której umieszczana jest zawiesina komórek. Dokładne monitorowanie tempa zamrażania pomaga zapobiegać szybkiemu odwodnieniu komórkowemu i tworzeniu się kryształków lodu. Zasadniczo komórki są pobierane z temperatury pokojowej do około -90 ° C (-130 ° F) w zamrażarce o kontrolowanej prędkości. Zawiesinę zamrożonych komórek przenosi się następnie do zamrażarki z ciekłym azotem utrzymywanej w ekstremalnie niskich temperaturach z azotem w fazie pary lub w fazie ciekłej. Kriokonserwacja oparta na liofilizacji nie wymaga użycia zamrażarek z ciekłym azotem.
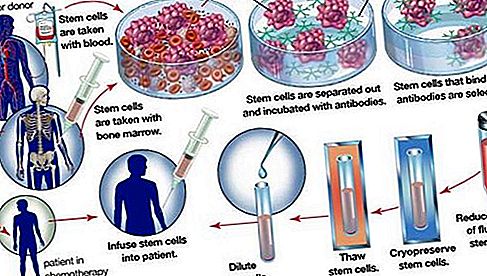
Ważnym zastosowaniem kriokonserwacji jest zamrażanie i przechowywanie hematopoetycznych komórek macierzystych, które znajdują się w szpiku kostnym i krwi obwodowej. W ratowaniu autologicznego szpiku kostnego krwiopochodne komórki macierzyste są pobierane ze szpiku kostnego pacjenta przed leczeniem chemioterapią dużymi dawkami. Po leczeniu zamrożone komórki pacjenta rozmraża się i wlewa z powrotem do organizmu. Ta procedura jest konieczna, ponieważ chemioterapia wysokodawkowa jest niezwykle toksyczna dla szpiku kostnego. Zdolność do kriokonserwacji krwiotwórczych komórek macierzystych znacznie poprawiła wyniki leczenia niektórych chłoniaków i nowotworów litych nowotworów. W przypadku pacjentów z białaczką ich komórki krwi są rakowe i nie można ich wykorzystywać do autologicznego ratowania szpiku kostnego. W rezultacie pacjenci ci polegają na kriokonserwowanej krwi pobranej z pępowiny noworodków lub na kriokonserwowanych krwiotwórczych komórkach macierzystych uzyskanych od dawców. Od późnych lat 90. XX wieku uznano, że krwiopochodne komórki macierzyste i mezenchymalne komórki macierzyste (pochodzące z embrionalnej tkanki łącznej) są zdolne do różnicowania się w tkanki mięśni szkieletowych i sercowych, tkanki nerwowej i kości. Obecnie istnieje duże zainteresowanie wzrostem tych komórek w systemach hodowli tkankowej, a także kriokonserwacją tych komórek w celu przyszłej terapii wielu różnych zaburzeń, w tym zaburzeń układu nerwowego i mięśniowego oraz chorób wątroby i serca.
Kriokonserwacja służy również do zamrażania i przechowywania ludzkich zarodków i nasienia. Jest to szczególnie cenne w przypadku zamrażania dodatkowych zarodków wytwarzanych przez zapłodnienie in vitro (IVF). Para może zdecydować się na użycie zarodków poddanych cytrozach w późniejszych ciążach lub w przypadku niepowodzenia IVF w przypadku świeżych zarodków. W procesie przenoszenia zamrożonego zarodka zarodki są rozmrażane i wszczepiane do macicy kobiety. Przeniesienie zamrożonego zarodka wiąże się z niewielkim, ale znaczącym wzrostem ryzyka raka dzieciństwa u dzieci urodzonych z takich zarodków.
Głęboka hipotermia, forma łagodnej kriokonserwacji stosowana u ludzi, ma znaczące zastosowania. Powszechnym zastosowaniem indukcji głębokiej hipotermii są skomplikowane zabiegi chirurgiczne układu krążenia. Po umieszczeniu pacjenta na całkowitym obejściu krążeniowo-oddechowym za pomocą maszyny serce-płuco krew przechodzi przez komorę chłodzącą. Kontrolowane chłodzenie pacjenta może osiągnąć wyjątkowo niskie temperatury około 10–14 ° C (50–57 ° F). Ta ilość chłodzenia skutecznie zatrzymuje wszelką aktywność mózgową i zapewnia ochronę wszystkich ważnych narządów. Po osiągnięciu tego ekstremalnego chłodzenia można zatrzymać maszynę płuco-serce, a chirurg może naprawić bardzo złożone wady aorty i serca podczas zatrzymania krążenia. W tym czasie w ciele pacjenta nie krąży krew. Po zakończeniu operacji krew stopniowo ogrzewa się w tym samym wymienniku ciepła, który służy do chłodzenia. Stopniowe ocieplenie z powrotem do normalnej temperatury ciała powoduje wznowienie normalnych funkcji mózgu i narządów. Ta głęboka hipotermia jest jednak daleka od zamrożenia i długotrwałej kriokonserwacji.
Komórki mogą żyć ponad dekadę, jeśli są odpowiednio zamrożone. Ponadto niektóre tkanki, takie jak gruczoły przytarczyczne, żyły, zastawki serca i tkanka aorty, można skutecznie zamrozić. Zamrażanie służy również do przechowywania i utrzymania długoterminowej żywotności wczesnych ludzkich zarodków, komórek jajowych (jaj) i nasienia. Procedury zamrażania stosowane dla tych tkanek są dobrze ustalone, a w obecności środków krioprotekcyjnych tkanki mogą być przechowywane przez długi czas w temperaturze -14 ° C (6,8 ° F).
Badania wykazały, że całe zwierzęta zamrożone przy braku środków krioprotekcyjnych mogą uzyskać żywe komórki zawierające nienaruszony DNA po rozmrożeniu. Na przykład jądra komórek mózgowych z całych myszy przechowywane w temperaturze -20 ° C (-4 ° F) przez ponad 15 lat zostały wykorzystane do wygenerowania linii embrionalnych komórek macierzystych. Komórki te następnie wykorzystano do wytworzenia mysich klonów.







![Rewolucja irańska [1978–1979] Rewolucja irańska [1978–1979]](https://images.thetopknowledge.com/img/world-history/8/iranian-revolution-19781979.jpg)





