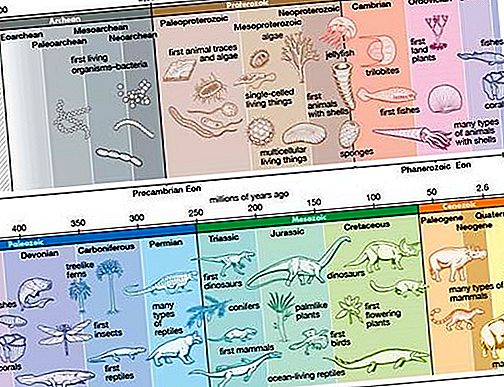
Właściwości fizyczne
Woda ma kilka ważnych właściwości fizycznych. Chociaż te właściwości są znane ze względu na wszechobecność wody, większość fizycznych właściwości wody jest dość nietypowa. Biorąc pod uwagę niską masę molową składowych cząsteczek, woda ma niezwykle duże wartości lepkości, napięcia powierzchniowego, ciepła odparowywania i entropii odparowywania, które można przypisać rozległym interakcjom wiązania wodorowego obecnym w ciekłej wodzie. Otwarta struktura lodu, która pozwala na maksymalne wiązanie wodoru, wyjaśnia, dlaczego woda stała jest mniej gęsta niż woda płynna - wysoce niezwykła sytuacja wśród popularnych substancji.
| Wybrane właściwości fizyczne wody | |
|---|---|
| masa cząsteczkowa | 18,0151 gramów na mol |
| temperatura topnienia | 0,00 ° C |
| temperatura wrzenia | 100,00 ° C |
| maksymalna gęstość (w 3,98 ° C) | 1,0000 gramów na centymetr sześcienny |
| gęstość (25 ° C) | 0,99701 gramów na centymetr sześcienny |
| prężność pary (25 ° C) | 23,75 torr |
| ciepło topnienia (0 ° C) | 6,010 kilodżuli na mol |
| ciepło parowania (100 ° C) | 40,65 kilodżuli na mol |
| ciepło formowania (25 ° C) | -285.85 kilodżuli na mol |
| entropia parowania (25 ° C) | 118,8 dżula na mol ° C |
| lepkość | 0,8903 centipoise |
| napięcie powierzchniowe (25 ° C) | 71,97 dyn na centymetr |
Właściwości chemiczne
Reakcje kwasowo-zasadowe
Woda ulega różnego rodzaju reakcjom chemicznym. Jedną z najważniejszych chemicznych właściwości wody jest jej zdolność do zachowywania się zarówno jako kwas (donor protonu), jak i zasada (akceptor protonu), charakterystyczna właściwość substancji amfoterycznych. To zachowanie jest najwyraźniej widoczne w autojonizacji wody: H 2 O (l) + H 2 O (l) ⇌ H 3 O + (aq) + OH - (aq), gdzie (l) reprezentuje stan ciekły, (aq) oznacza, że gatunki są rozpuszczone w wodzie, a podwójne strzałki wskazują, że reakcja może zachodzić w obu kierunkach i istnieją warunki równowagi. W temperaturze 25 ° C (77 ° F) do stężenia uwodnionego H + (tj H 3 O +, znany jako jonu hydroniowego) w wodzie wynosi 1,0 x 10 -7 m, gdzie M oznacza mola na litr. Ponieważ jeden OH - jonowa wytwarzana jest przez każdego H 3 O + jonową, stężenie OH - w temperaturze 25 ° C jest również 1,0 x 10 -7 M. w wodzie o temperaturze 25 ° C H 3 O + stężenie i OH - stężenie musi zawsze wynosić 1,0 × 10 −14: [H +] [OH -] = 1,0 × 10 −14, gdzie [H +] oznacza stężenie uwodnionych jonów H + w molach na litr, a [OH -] oznacza stężenie OH - jony w molach na litr.
Kiedy kwas (substancja, która może wytwarzać jony H +) rozpuszcza się w wodzie, zarówno kwas, jak i woda przyczyniają się do roztworu jonów H +. Prowadzi to do sytuacji, w której stężenie H + jest większe niż 1,0 × 10–7 M. Ponieważ zawsze musi być prawdą, że [H +] [OH -] = 1,0 × 10 −14 w temperaturze 25 ° C, [OH -] należy obniżyć do wartości poniżej 1,0 × 10 −7. Mechanizm zmniejszania stężenia OH - polega na reakcji H + + OH - → H 2 O, który występuje w zakresie koniecznym do przywracania produktu z [H +] i [OH -] do 1,0 x 10 -14 M. Zatem po dodaniu kwasu do wody powstały roztwór zawiera więcej H + niż OH -; to jest, [H +]> [OH -]. Taki roztwór (w którym [H +]> [OH -]) jest określany jako kwasowy.
Najczęstszą metodą określania kwasowości roztworu jest jego pH, które definiuje się w kategoriach stężenia jonów wodoru: pH = -log [H +], gdzie log log oznacza logarytm zasady 10. W czystej wodzie, w której [H +] = 1,0 × 10–7 M, pH = 7,0. W przypadku kwaśnego roztworu pH wynosi mniej niż 7. Gdy zasada (substancja, która zachowuje się jak akceptor protonów) rozpuszcza się w wodzie, stężenie H + zmniejsza się, tak że [OH -]> [H +]. Roztwór podstawowy charakteryzuje się pH> 7. Podsumowując, w roztworach wodnych w temperaturze 25 ° C:
| neutralne rozwiązanie | [H +] = [OH -] | pH = 7 |
| kwaśny roztwór | [H +]> [OH -] | pH <7 |
| podstawowe rozwiązanie | [OH -]> [H +] | pH> 7 |