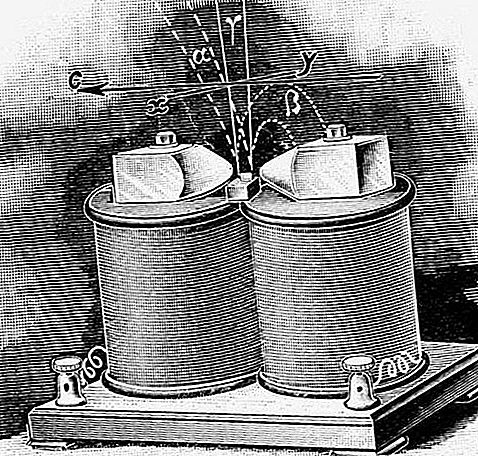
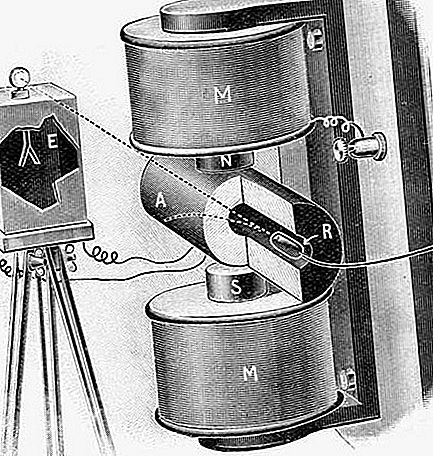
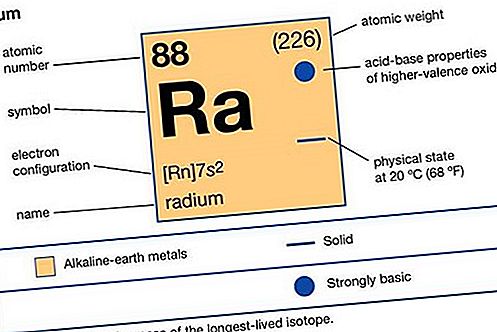
Rad (Ra), radioaktywny pierwiastek chemiczny, najcięższy z metali ziem alkalicznych z grupy 2 (IIa) układu okresowego pierwiastków. Rad jest srebrzystym białym metalem, który nie występuje w naturze jako wolny.

metali ziem alkalicznych
bar (Ba) i rad (Ra).
Właściwości elementu
| Liczba atomowa | 88 |
|---|---|
| najstabilniejszy izotop | 226 |
| temperatura topnienia | około 700 ° C (1300 ° F) |
| temperatura wrzenia | nie ustalony (około 1100–1 700 ° C [2 000–3 100 ° F]) |
| środek ciężkości | około 5 |
| stan utlenienia | +2 |
| konfiguracja elektronów | [Rn] 7s 2 |
Występowanie, właściwości i zastosowania
Rad został odkryty (1898) przez Pierre'a Curie, Marie Curie i asystenta, G. Bémonta, po tym, jak Marie Curie zauważyła, że radioaktywność pitchblende była cztery lub pięć razy większa niż zawartego w nim uranu i nie została w pełni wyjaśniona na podstawa radioaktywnego polonu, którą właśnie odkryła w pozostałościach bladopłetwych. Nową, silnie radioaktywną substancję można było skoncentrować barem, ale ponieważ jego chlorek był nieco bardziej nierozpuszczalny, można go wytrącić przez krystalizację frakcyjną. Po oddzieleniu nastąpił wzrost intensywności nowych linii w widmie ultrafioletowym i stały wzrost pozornej masy atomowej materiału, aż do uzyskania wartości 225,2, co jest wartością zbliżoną do obecnie przyjętej wartości 226,03. Do 1902 r. Przygotowano 0,1 grama czystego chlorku radu przez rafinację kilku ton pozostałości smoły sklejonej, a do 1910 r. Marie Curie i André-Louis Debierne wyodrębnili sam metal.
Znane są trzydzieści cztery izotopy radu, wszystkie radioaktywne; ich okres półtrwania, z wyjątkiem radu-226 (1600 lat) i radu-228 (5,75 lat), jest krótszy niż kilka tygodni. Długowieczny rad-226 występuje w naturze w wyniku jego ciągłego powstawania w wyniku rozpadu uranu-238. W ten sposób rad występuje we wszystkich rudach uranu, ale jest szerzej rozpowszechniony, ponieważ tworzy związki rozpuszczalne w wodzie; Powierzchnia Ziemi zawiera około 1,8 × 10 13 gramów (2 × 10 7 ton) radu.
Ponieważ wszystkie izotopy radu są radioaktywne i krótkotrwałe w geologicznej skali czasu, pierwotny rad zniknąłby dawno temu. Dlatego rad występuje naturalnie tylko jako produkt rozpadu w trzech naturalnych seriach rozpadu promieniotwórczego (szereg toru, uranu i aktynu). Rad-226 jest członkiem serii rozpadu uranu. Jego rodzicem jest tor-230 i jego córka radon-222. Dalszymi produktami rozpadu, wcześniej zwanymi radem A, B, C, C ', C ″, D itd., Są izotopy polonu, ołowiu, bizmutu i talu.