Pasma energetyczne
Metale
Elektrony walencyjne, które w innych substancjach wytwarzają wiązania między poszczególnymi atomami lub małymi grupami atomów, są równo dzielone przez wszystkie atomy w kawałku metalu. Te zdelokalizowane elektrony mogą zatem przemieszczać się po całym kawałku metalu i zapewniać połysk metalu oraz dobre przewodnictwo elektryczne i cieplne metali i stopów. Teoria pasm wyjaśnia, że w takim systemie poszczególne poziomy energii są zastępowane ciągłym regionem zwanym pasmem, jak na wykresie gęstości stanów miedzi miedzi pokazanym na rysunku. Ten schemat pokazuje, że liczba elektronów, które mogą być umieszczone w paśmie przy dowolnej danej energii, jest różna; w miedzi liczba ta maleje, gdy pasmo zbliża się do wypełnienia elektronami. Liczba elektronów w miedzi wypełnia pasmo do pokazanego poziomu, pozostawiając pustą przestrzeń przy wyższych energiach.
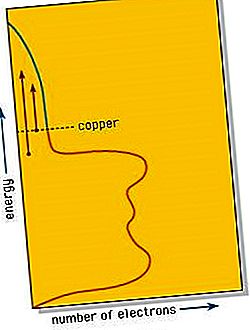
Gdy foton światła jest absorbowany przez elektron blisko szczytu pasma energii, elektron jest podnoszony do wyższego dostępnego poziomu energii w paśmie. Światło jest tak intensywnie pochłaniane, że może przenikać na głębokość zaledwie kilkuset atomów, zwykle mniej niż jedną długość fali. Ponieważ metal jest przewodnikiem elektryczności, pochłonięte światło, które jest przecież falą elektromagnetyczną, indukuje przemienne prądy elektryczne na powierzchni metalu. Prądy te natychmiast ponownie emitują foton z metalu, zapewniając tym samym silne odbicie wypolerowanej metalowej powierzchni.
Wydajność tego procesu zależy od pewnych zasad selekcji. Jeśli skuteczność absorpcji i reemisji jest w przybliżeniu równa przy wszystkich energiach optycznych, wówczas różne kolory białego światła będą równie dobrze odbijane, co prowadzi do „srebrzystego” koloru polerowanych powierzchni srebra i żelaza. W miedzi efektywność odbicia maleje wraz ze wzrostem energii; zmniejszone odbicie na niebieskim końcu widma powoduje czerwonawy kolor. Podobne rozważania wyjaśniają żółty kolor złota i mosiądzu.
Czyste półprzewodniki
W wielu substancjach pasmo wzbronione pojawia się na wykresie gęstości stanów (patrz rysunek). Może się to zdarzyć, na przykład, gdy w czystej substancji znajdują się średnio dokładnie cztery elektrony walencyjne na atom, co powoduje powstanie całkowicie pełnego dolnego pasma, zwanego pasmem walencyjnym, i dokładnie pustego górnego pasma, pasma przewodzenia. Ponieważ w szczelinie między dwoma pasmami nie ma poziomów energii elektronów, światło o najniższej energii, które można zaabsorbować, odpowiada strzałce A na rysunku; reprezentuje to wzbudzenie elektronu od szczytu pasma walencyjnego do dołu pasma przewodzenia i odpowiada energii pasma-szczeliny oznaczonej Eg. Światło o dowolnej wyższej energii może być również pochłaniane, jak wskazują strzałki B i C.
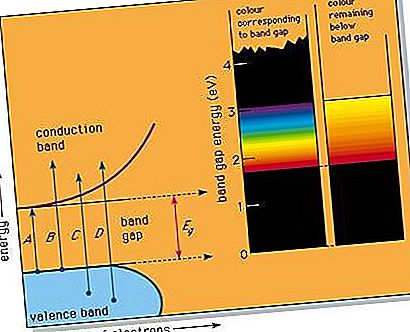
Jeśli substancja ma dużą przerwę pasmową, taką jak 5,4 eV diamentu, wówczas światło w widmie widzialnym nie może zostać zaabsorbowane, a substancja wydaje się bezbarwna, gdy jest czysta. Takie półprzewodniki o dużych odstępach pasma są doskonałymi izolatorami i częściej są traktowane jako materiały jonowe lub kowalencyjnie związane.
Pigment kadmowo żółty (siarczek kadmu, znany również jako mineralny greenockit) ma mniejszą przerwę pasmową wynoszącą 2,6 eV, co pozwala na absorpcję fioletu i niektórych niebieskich, ale nie ma innych kolorów. Prowadzi to do jego żółtego koloru. Nieco mniejsza przerwa pasmowa, która pozwala na absorpcję fioletu, niebieskiego i zielonego, daje kolor pomarańczowy; jeszcze mniejsza szczelina pasmowa jak w 2,0 eV cynobru pigmentowego (siarczek rtęci, cynober mineralny) powoduje, że wszystkie energie, ale czerwień jest absorbowana, co prowadzi do czerwonego koloru. Całe światło jest absorbowane, gdy energia pasma wzbronionego jest mniejsza niż granica 1,77-eV (700 nm) widma widzialnego; półprzewodniki o wąskim paśmie wzbronionym, takie jak galena z siarczkiem ołowiu, pochłaniają zatem całe światło i są czarne. Ta sekwencja bezbarwnych, żółtych, pomarańczowych, czerwonych i czarnych jest dokładną gamą kolorów dostępnych w czystych półprzewodnikach.
Domieszkowane półprzewodniki
Jeśli atom zanieczyszczenia, często nazywany domieszką, jest obecny w półprzewodniku (który jest następnie oznaczany jako domieszkowany) i ma inną liczbę elektronów walencyjnych niż atom, który zastępuje, w poziomie pasma mogą powstać dodatkowe poziomy energii. Jeśli zanieczyszczenie ma więcej elektronów, takich jak zanieczyszczenie azotem (pięć elektronów walencyjnych) w krysztale diamentu (składającym się z atomów węgla, każdy mający cztery elektrony walencyjne), powstaje poziom dawcy. Elektrony z tego poziomu mogą być wzbudzane do pasma przewodzenia przez absorpcję fotonów; występuje to tylko na niebieskim końcu widma w diamentie domieszkowanym azotem, co daje komplementarny żółty kolor. Jeśli zanieczyszczenie ma mniej elektronów niż atom, który zastępuje, takie jak zanieczyszczenie borem (trzy elektrony walencyjne) w diamentie, powstaje poziom dziury. Fotony mogą być teraz pochłaniane przez wzbudzenie elektronu z pasma walencyjnego do poziomu otworu. W przypadku diamentu z domieszką boru dzieje się to tylko na żółtym końcu widma, co daje ciemnoniebieski kolor, jak w słynnym diamentu Hope.
Niektóre materiały zawierające zarówno donory, jak i akceptory mogą pochłaniać promieniowanie ultrafioletowe lub elektryczne w celu wytworzenia światła widzialnego. Na przykład proszki luminoforu, takie jak siarczek cynku zawierający miedź i inne zanieczyszczenia, stosuje się jako powłokę w lampach fluorescencyjnych w celu przekształcenia dużej ilości energii ultrafioletowej wytwarzanej przez łuk rtęciowy w światło fluorescencyjne. Fosfory są również używane do pokrywania wnętrza ekranu telewizora, gdzie są one aktywowane przez strumień elektronów (promieni katodowych) w katodoluminescencji oraz w farbach świecących, gdzie są one aktywowane przez światło białe lub promieniowanie ultrafioletowe, co powoduje, że wykazują powolny zanik światła znany jako fosforescencja. Elektroluminescencja wynika ze wzbudzenia elektrycznego, tak jak proszek fosforowy osadza się na metalowej płytce i pokrywa przezroczystą elektrodą przewodzącą w celu wytworzenia paneli oświetleniowych.
Elektroluminescencja wtryskowa zachodzi, gdy kryształ zawiera połączenie między różnymi domieszkowanymi obszarami półprzewodnikowymi. Prąd elektryczny wytworzy przejścia między elektronami i dziurami w obszarze połączenia, uwalniając energię, która może pojawić się jako światło prawie monochromatyczne, podobnie jak w diodach elektroluminescencyjnych (LED) szeroko stosowanych w urządzeniach wyświetlających w sprzęcie elektronicznym. Przy odpowiedniej geometrii emitowane światło może być również monochromatyczne i spójne, jak w laserach półprzewodnikowych.